(https://minzdrav.gov.ru/news/2Q20/Q8/11/14657-minzdrav-rossii-zaregistriroval-pervuyu-v-mire- vaktsinu-ot-covid-19 и другие). Но благодаря вакцинации обеспечивается колоссальное преимущество, поскольку вакцина позволяет сформировать иммунитет без заболевания и его осложнений. Кроме того, ожидается, что поствакцинальный иммунитет будет более сильным, чем постинфекционный, поскольку иммунный ответ на вакцину является более избирательным и мощным, чем при естественном инфицировании.
Вакцины, применяемые в нашей стране индуцируют как гуморальный, так и клеточный иммунитет в отношении SARS-CoV-2.
Согласно Национальному плану мероприятий по вакцинации против инфекции COVID-19 в Республике Беларусь на 2021-2022 годы, ставится задача охватить прививками не менее 60% населения как страны в целом, так и каждого региона.
Справочно 1: Вакцинация формирует индивидуальную защиту привитого человека, предупреждает возникновение заболевания, его тяжелое течение и неблагоприятный исход. Но если охват населения будет менее 60%, то мы не сможем сформировать «коллективную защиту» и не сможем повлиять на интенсивность распространения вируса. В настоящее время продолжают проводиться исследования и возможно изменение поставленной задачи при получении новых данных.
Справочно 2: По данным CDC с увеличением возраста существенно увеличивается риск госпитализации и летального исхода в результате COVID-19:
Примечание: При сопоставлении с группой сравнения, количество случаев (госпитализаций, летальных исходов) в других группах было аналогичным (=) или умноженным на 2, 3200, 8700 и т.д. Т.е. в возрастной группе 85 лет и старше количество случаев выше в 2 раза, количество госпитализаций выше в 95 раз, а количество летальных исходов выше в 8700 раз по сравнению с аналогичными данными в возрастной группе 5-17 лет.
Данные эпидемиологического надзора за COVID-19, поступившие из 21 страны Европейского региона ВОЗ свидетельствуют о корреляции между повышением охвата вакцинацией и снижением смертности в определенных возрастных группах. При условии вакцинации более 50% всего населения к середине сентября 2021 года можно предотвратить значительное число случаев инфекции, госпитализаций и летальных исходов, причем наибольшее количество предотвращенных госпитализаций и летальных исходов будет среди населения в возрасте 60 лет и старше, а наибольшее количество предотвращенных случаев заболевания будет среди лиц моложе 60 лет. Если к концу 2021 года охват вакцинацией увеличится с 50% до 80%, то можно дополнительно
предотвратить до 11%) летальных исходов (Внеочередное совещание Европейской технической консультативной группы экспертов по иммунизации (ЕТКГЭ) 28.04.2021, Европейское бюро ВОЗ).
1.5. Проводится ли в нашей стране изучение циркулирующих вариантов вируса, позволяет ли эта система установить наличие в циркуляции мутировавших штаммов?
Циркулирующие на территории нашей страны варианты вируса SARS-CoV-2 изучают в ГУ «Республиканский научно-практический центр эпидемиологии и микробиологии». Здесь проводится выделение вируса и секвенирование участка генома, который позволяет установить наличие мутаций. Таким образом, регулярный мониторинг и оценка эпидемиологической значимости циркулирующих на территории Республики Беларусь проводится.
1.6. Защищает ли вакцинация, проведенная с использованием вакцин против COVID-19, от заражения мутировавшими вариантами вируса SARS-CoV-2, известными в настоящее время?
Исследования в этом направлении продолжаются.
Результаты уже имеющихся исследований (в том числе, и по вакцине Гам-КОВИД-Вак), свидетельствуют, что имеет место снижение эффективности вакцинации (снижение уровня нейтрализации) например, к варианту дельта (В. 1.617.2), но это снижение не влияет на главное - на уровень защиты в предупреждении тяжелого течения инфекции, госпитализации и летального исхода, который дает полная вакцинация
В настоящем периоде исследований ученые не выявили escape- мутантов, которые по-настоящему «ускользают» от действия нейтрализующих антител. Пока в технологии производства вакцин используется формат полноразмерного спайк-белка. Такую ситуацию, чтобы штамм вируса полностью «ускользал» от иммунной системы, представить СЛОЖНО По данным ВОЗ, в ходе обсервационного исследования среди штамма (Р.1) приходилось 75% образцов SARS-CoV-2, эпидемиологическая эффективность защиты от симптоматического течения инфекции, обеспечиваемой инактивированной цельновирионной вакциной Sinovac-CoronaVac, разработанной компанией «Синовак»/Китайской национальной фармацевтической группой для профилактики COVID-19, составила, по оценкам, 49,6%.
В районах с широкомасштабной циркуляцией значимого варианта Р.2 (также на территории Бразилии) эффективность вакцины оценивалась на уровне 49,6% после введения как минимум одной дозы и была зарегистрирована на уровне 50,7% по истечении двух недель после второй дозы. В настоящее время Стратегическая консультативная группа экспертов ВОЗ по иммунизации (СКГЭ) рекомендует применять данную вакцину в рамках дорожной карты ВОЗ по приоритетному порядку использования вакцин
Раздел 2. Особенности создания и применения вакцин против COVID-19
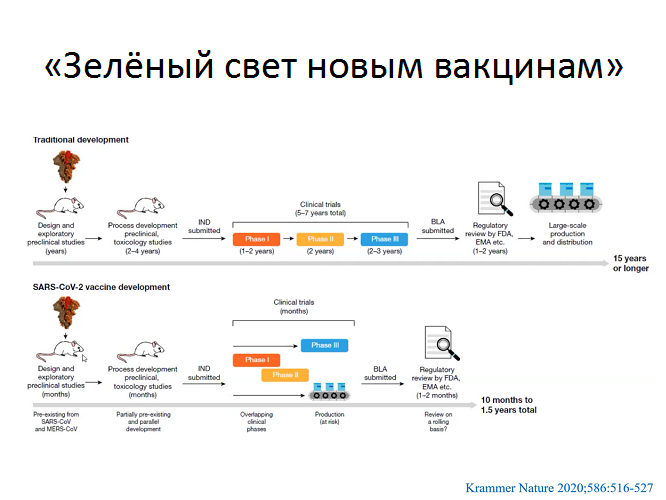
Как получилось разработать вакцины против COVID-19 с такой рекордной скоростью, при этом обеспечив их качество и безопасность?
В течение последних 10-15 лет создание новых вакцинных препаратов идет по пути не только усовершенствования классических технологий, но и в большей степени, использования известных научных разработок в области геномики и протеомики. Такие исследования проводятся очень интенсивно применительно к медицине, ветеринарии и фундаментальной науке. Новые подходы достаточно унифицированы просты и дешевы, и позволяют получать вакцины в значительно больших количествах, кроме того, они исключают работу с инфекционным материалом в процессе производства, а следовательно являются безопасными для вакцинируемых.Из-за чрезвычайности ситуации в условиях пандемии, в экстренном порядке, благодаря международному сотрудничеству появилась возможность ускорять исследования и клинические испытания. Для традиционной разработки вакцин необходим был срок до 10-15 лет от момента создания до промышленного производства и использования. Из них только клинические испытания занимали 5-7 лет, фазы клинических испытаний не пересекались. При разработке вакцин против COVID-19 для ускорения их создания пересекались фазы 1 и 2, 2 и 3. Сочетание следующих факторов позволило быстро разработать вакцины против COVID-19, обеспечив при этом их качество и безопасность:
- Разработка этих вакцин являлась приоритетной задачей в условиях чрезвычайной ситуации в мире в связи с пандемией, поэтому темпы разработки были ускорены за счет одномоментного проведения первой и второй фаз испытаний. Регуляторные органы оперативно проводили анализ каждой фазы испытания.
- Разработка велась с использованием последних научнотехнических достижений: как на основе ранее отработанных
технологических платформ (векторные, инактивированные цельновирионные вакцины), так и с использованием новых технологических платформ (мРНК-вакцины).
- Инвесторы задолго до окончания клинических испытаний подготовились к производству, что позволило в кратчайшие сроки обеспечить наработку значительных объемов препаратов.
2.1. Какова эффективность вакцин против COVID-19, применяемых в Республике Беларусь?
Эффективность вакцины Гам-КОВИД-Вак (РФ) на уровне 91,6% (рассчитана на основании данных о заболевании COVID-19 19866 добровольцев, разделенных случайным образом на 2 группы -
получивших полный курс вакцинации (2 инъекции) или получивших плацебо).
В последующем, по результатам оценки среди 3,8 млн россиян,
получивших вакцинацию, эффективность составила 97,6%.
Вакцина Г ам-КОВИД-Вак формирует высокий уровень
поствакцинальных антител, обеспечивающих достаточную защиту от клинически выраженных форм COVID-19, что показано в сравнительных исследованиях.
Эффективность вакцинации с использованием инактивированной вакцины (КНР) составляет около 70% (в предупреждении заражения вирусом SARS-CoV-2).
Обе вакцины индуцируют как гуморальный, так и клеточный иммунитет в отношении SARS-CoV-2. Предупреждают возникновение тяжелых случаев заболевания (предупреждают госпитализацию) и летальный ИСХОД.
Применяемые в нашей стране вакцины обеспечивают положительное воздействие как на гуморальный (образование антител), так и на клеточный (специфическая активация Т-клеток) иммунитет в отношении коронавируса. Вакцинация ведет к выработке эффективной и продолжительной иммунологической памяти, которая обеспечивает защиту от инфекции и после утраты антител.
В этой связи необходимо отметить, что результаты определения уровня поствакцинальных антител не позволят в полной мере оценить защищенность от заболевания, поэтому поствакцинальное определение титра антител считается нецелесообразным (CDC, 2021).
2.2. Могут ли вакцины против COVID-19 негативно влиять на репродуктивную функцию?
Нет никаких доказательств того, что вакцины, в том числе, вакцины против COVID-19, могут оказывать негативное влияние на репродуктивную функцию мужчин или женщин. Беременные женщины переносят заболевание COVID-19 хуже, по сравнению с другими людьми их возраста, они чаще испытывают осложнения беременности, такие как выкидыш, мертворождение, образование тромбов и преждевременные роды. В настоящее время нет никаких веских причин - медицинских или научных механизмов - для утверждения того, что используемые вакцины взаимодействуют с репродуктивными органами женщины или влияют на яйцеклетки. Вакцинация рекомендуется также мужчинам, озабоченным своей фертильностью из-за возможных последствий болезни COVID-19 для их репродуктивной системы.
Раздел 3. Назначение вакцинации. Общие рекомендации.
3.1. Каковы интервалы для планирования на иммунизацию после перенесенной коронавирусной инфекцией?
Вакцинация против COVID-19 рекомендована всем переболевшим, вне зависимости от формы и степени тяжести заболевания.
Данные многих объёмных исследований П/Ш фазы подтверждают безопасность и эффективность вакцинации у переболевших.
Вакцинация может быть сделана после выздоровления пациента (в зависимости от тяжести течения можно провести вакцинацию-1 или вакцинацию-2 через 2-8 недель после выздоровления). Доказательных данных о наличии минимального интервала между выздоровлением и вакцинацией нет.
Исключение: применение моноклональных антител в терапии
COVID-19 - у таких пациентов целесообразно выдержать интервал 90 дней после введения и до вакцинации (на основании периода полу выведения и отсутствия данных о безопасности).
В то же время, необходимо учитывать, что в условиях, когда охваты населения вакцинацией не велики, целесообразно отложить проведение вакцинации переболевших на 3-6 месяцев после COVID-19. Это позволит охватить вакцинацией в первую очередь тех людей, которые не болели и, риск возникновения заболевания у которых выше при столкновении с источником инфекции по сравнению с переболевшими.
Если пациент получил вакцинацию компонентом I (вакцинацию-1), затем перенес COVID-19, то введение компонента II (проведение вакцинации-2) проводится после его выздоровления (в зависимости от тяжести течения можно провести вакцинацию-1 через 2-8 недели после выздоровления).
Уровень системных реакций на введение первой дозы вакцины против COVID-19 у лиц, имеющих антитела к вирусу до вакцинации может быть выше и выраженность реакций может быть интенсивнее, по сравнению с лицами, которые были серонегативны до вакцинации. На введение второй дозы ситуация противоположная: наибольший уровень и интенсивность реакций может быть у серонегативных до вакцинации
3.2. Если в интервале между введением первого и второго компонентов возникло острое заболевание или обострение хронического заболевания.
Введение второго компонента необходимо провести после выздоровления при остром заболевании или начала стадии ремиссии при хроническом заболевании. В индивидуальных случаях возможно предусмотреть введение второго компонента через 2-4 недели после выздоровления при остром заболевании или начала стадии ремиссии при хроническом заболевании (в зависимости от тяжести перенесенного заболевания, но сопоставляя с риском возникновения COVID-19, риском его тяжелого течения).
Максимальный интервал между введениями компонентов не регламентирован. В тоже время, имеется ряд исследований, которые показали, что увеличение интервала между введением компонентов вакцины Гам-КОВИД-Вак (РФ) до 90 дней, между введение доз инактивированной вакцины (КНР) до 56 дней не приводили к существенному снижению иммуногенности по сравнению с контрольными группами, получавшими компоненты (дозы) с минимальным интервалом
3.3. Насколько целесообразно проведение обследование на наличие антигена или антител к вирусу SARS-CoV-2?
Целесообразность обследования перед проведением вакцинации на наличие антигена или антител к вирусу SARS-CoV-2 отсутствует, т. к. не несет в себе никакой конкретной информации для принятия решения (наличие определенного уровня антител не свидетельствует об определенном уровне защиты). В настоящий момент не определен защитный уровень антител (гуморальный иммунитет): работы по определению этого параметра находятся в стадии исследований и пока не приняты, в том числе ВОЗ. Имеющиеся в настоящий момент тест-системы для определения клеточного иммунитета не могут рекомендоваться для рутинных исследований из-за отсутствия достоверных данных по интерпретации результатов (длительность защиты, ее выраженность и т.д.).
3.4. Если обследование на наличие антител было проведено (по другим причинам) и имеются данные о наличии Ig G (качественный тест) или титров не ниже защитного Ig G (количественный тест), назначается ли вакцинация?
Наличие определенного количества вируснейтрализующих антител класса IgG к SARS-CoV-2 у переболевших не гарантирует защиту от повторного заражения уже через 3-6 месяцев после ранее перенесенной инфекции, поэтому вакцинация показана и данной категории населения. При этом введение вакцины позволит сформировать более стойкий иммунитет.
Риск повторного инфицирования в ближайшие 3-6 месяцев после болезни невысокий. По истечении данного времени целесообразно запланировать вакцинацию.
Результаты зарегистрированных в настоящее время тестов на антитела к SARS-CoV-2 не должны использоваться для оценки уровня защиты человека ОТ COVID-19 (официальная позиция FDA 19 мая 2021 года).
3.5. Являются ли аллергические реакции в прошлом на введение каких-либо лекарственных средств, пищевых продуктов противопоказанием к вакцинации?
Вакцины, как и любое другое лекарственное средство, могут вызывать аллергические реакции разной степени тяжести - от легких до тяжелых - у лиц с очень высокой чувствительностью к активному веществу или любому из компонентов вакцины. Данные по безопасности, полученные в ходе клинических испытаний, не указывают на какой-либо повышенный риск развития аллергической реакции, но при этом, учитывая ограниченное количество доз вакцин, введенных к настоящему моменту, очень редкие аллергические реакции (что означает менее 1 случая на 10000 вакцинированных лиц) все же нельзя исключить (ВОЗ, Разъяснения по поводу вакцин против COVID-19). В качестве общего правила при использовании любых вакцин, вводимых парентерально, должно быть обеспечено незамедлительное оказание медицинской помощи, если это потребуется, и гарантировано наблюдение после вакцинации в течение не менее 30 минут.
3.6. Какие есть противопоказания к введению вакцины у лиц с хроническими заболеваниями?
Противопоказанием к вакцинации является обострение хронического заболевания. В таком случае назначение профилактической прививки возможно через 2-4 недели после ремиссии.
Прием лекарственных препаратов, угнетающих функцию иммунной системы является временным (относительным) противопоказанием к вакцинации. Безопасность вакцинации на фоне иммуносупрессивной терапии аналогична общей популяции. Эффективность может быть снижена. Для повышения эффективности вакцинации рекомендуется прекратить прием иммуносупрессивных препаратов или снизить интенсивность иммуносупрессии как минимум за 2 недели до и после вакцинации (по решению профильного консилиума).
Злокачественные новообразования не являются противопоказанием к вакцинации. Так как риск тяжелого течения инфекции COVID-19 в группе онкологических и гематологических пациентов существенно выше в сравнении с общей популяцией, то данные пациенты нуждаются в вакцинации, предпочтительно в интервалах между курсами химиотерапии и/или лучевой терапии (по решению консилиума с участием врача- инфекциониста и профильного врача-специалиста).
В Общей характеристике лекарственного препарата указано, что при наличии хронических заболеваний вакцинация проводится «с осторожностью». Пациент должен быть на базисной терапии, привержен к ней, быть в стойкой ремиссии - это главное условие для вакцинации. В таких ситуациях допуск на вакцинацию может быть согласован с лечащим врачом (со специалистом по профилю хронической патологии, консилиумом специалистов). Принятие решения о вакцинации каждого такого пациента должно основываться на оценке соотношения пользы и риска.
3.7. Необходимо ли проведение лабораторных исследований перед назначением вакцины (OAK, ОАМ, БАК)?
Назначение вакцинации каждому пациенту проводится врачом после его опроса, медицинского осмотра и изучения медицинского анамнеза.
Проведение лабораторного и/или диагностического исследования может потребоваться в отдельных случаях пациентам с хронической патологией, в целях оценки интенсивности (периода) протекания хронического заболевания.
На данном этапе нет необходимости проведения лабораторных исследований перед вакцинацией в рутинном порядке.
3.8. Как вакцинировать лиц, относящихся к контактам первого уровня?
Лиц, относившихся к контактам первого уровня можно вакцинировать не ранее окончания периода наблюдения, при отсутствии клинических проявлений заболевания. Их предварительное тестирование на наличие антигена или антител нецелесообразно.
3.9. Как осуществляется учет и проводится расследование поствакцинальных реакций? Как осуществлять наблюдение за привитыми?
Система наблюдения за привитыми и мониторинга за поствакцинальными реакциями установлена Санитарными нормами и правилами «Санитарно-эпидемиологические требования к транспортировке, хранению и использованию иммунобиологических лекарственных средств, проведению профилактических прививок, выявлению, регистрации и расследованию побочных реакций после профилактических прививок», утвержденными постановлением Министерства здравоохранения Республики Беларусь от 02 декабря 2013 №114.
Справочно: для предотвращения серьезных побочных реакций на профилактические прививки медицинский работник организации, проводивший профилактическую прививку, должен проводить наблюдение в течение 30 минут за пациентом, получившим профилактическую прививку, и далее в общем порядке оказания медицинской помощи пациентам.
После (в ходе) проведения медицинского наблюдения в случае выявления побочных реакций и заболеваний, регистрируемых с диагнозами и в сроки, установленные перечнем серьезных побочных реакций на профилактические прививки, подлежащих индивидуальной регистрации организациями здравоохранения, и сроками их выявления, проводится их регистрация и расследование в соответствии с требованиями ТИПА.
3.10. В медицинском осмотре пациента с оформлением результатов согласно приложению 4 к приказу Минздрава от №412 с изменениями, внесенными приказом Минздрава от №446, не предусмотрено медработнику, проводившему осмотр, при разрешении иммунизации указывать место и способ введения, дозу, наименование ИЛС, кратность иммунизации. При этом в случае расследования сильных и побочных реакций после профилактических прививок вышеуказанные данные имеют значение.
Сведения о месте и способе введения, дозе, наименование ИЛС, тип прививки (вакцинация-1 или вакцинация-2) вносятся в «Журнал учета профилактических прививок», сведения из которого должны
использоваться при проведении расследования случаев сильных побочных реакций после профилактических прививок.
3.11. Какие имеются возрастные ограничения для применения вакцины Гам-КОВИД-Вак?
Согласно инструкции по медицинскому применению (Общей характеристике лекарственного препарата) и листку-вкладышу: информация для пациента, вакцина Гам-КОВИД-Вак показана для профилактики COVID-19 у взрослых старше 18 лет.
3.12. Какова тактика иммунизации другими вакцинами (плановые и по эпидпоказаниям) по отношению к вакцинации против COVID-19?
Данные по одновременному введению с другими вакцинами в настоящее время изучаются. ВОЗ рекомендует странам продолжить проведение исследований по иммуногенности и безопасности при одновременном применении с другими вакцинами (включая вакцины от гриппа и пневмококковой инфекции) среди взрослых лиц. При накоплении достаточного объема данных ВОЗ даст рекомендации по этому вопросу. До получения таких данных следует соблюдать минимальный интервал в 2-4 недели между введением вакцины от
COVID-19 И любой другой вакцины (Разъяснения по поводу вакцин против COVID- 19, ВОЗ).
Лечебно-профилактический курс иммунизации против бешенства, экстренная профилактика столбняка проводятся по жизненным показаниям, независимо от того, за сколько времени до этого была начата (закончена) вакцинация против COVID-19.
3.13. Сроки допуска к донорству после вакцинации против COVID-19.
В соответствии с общепринятой мировой практикой сдача крови возможна не ранее чем через 30 дней после вакцинации с использованием вакцин, применяемых в нашей стране.
3.14. Может ли прививка повлиять на ложноположительный диагностический тест?
Вакцина не может повлиять на результаты ПЦР-теста или теста на антиген SARS-CoV-2 комбинированного назофарингеального мазка.
3.15. Является ли основанием для прерывания беременности факт вакцинации (если вакцинация была проведена в тот период, когда о беременности еще не было известно)?
В вакцинах, применяемых в Республике Беларусь, нет живого реплицирующегося материала. Накоплен опыт о тысячах женщин, которые были привиты в период беременности и еще не знали о ней. Установлено, что вакцинация не оказала влияния на плод. CDC не запрещает беременным вакцинацию, оставляя это решение на ИХ выбор
Раздел 4. Назначение вакцинации лицам с заболеваниями эндокринной системы
На сегодняшний день рекомендации по вакцинации против COVID-19 пациентов с различными заболеваниями эндокринной системы носят характер экспертного мнения, которое сформулировано на основании публикаций Международной федерации диабета, Европейского общества эндокринологов, Американской диабетологической ассоциации, американской тиреоидной ассоциации, ФБУ «НМИЦ эндокринологии» Минздрава России и др.
Подходы к вакцинации определяются рисками, которые ассоциированы с эндокринопатией.
Сахарный диабет (далее - СД).
Известно, что наличие СД является фактором риска более тяжелого течения COVID-19, что поддержано различными экспертными диабетологическими ассоциациями (JDRF, ADA и др.).
Бесспорно доказано, что исходы COVID-19 хуже у пациентов с СД, чем без него. Факторами, определяющими повышение риска негативного исхода COVID-19, являются возраст старше 65 лет, наличие ожирения, ХОБЛ или бронхиальной астмы, кардиоваскулярной патологии, хронической болезни почек. Люди с СД 1 и 2 типов, в 3 раза чаще нуждаются в госпитализации в связи с развитием тяжелого течения COVID-19. Это обусловлено гипергликемией, иммуносупрессией, усугубляющей риск развития деструктивного альвеолита, коагулопатией, увеличением распространенности сонного апноэ и нарушений вентиляции легких и другими факторами. Исследования, проведенные в 2020 году (Lancet Diabetes & Endocrinology), показали, ЧТО пациенты С СД чаще нуждаются в госпитализации и интенсивной терапии в результате развития острого
респираторного дистресс-синдрома, в 2-3 раза чаще умирают от COVID-19 в больнице, чем люди без диабета.
Согласно мнениям различных международных организаций и экспертов, пациентам с СД 1 и 2 типа рекомендуется прививаться от COVID-19, если нет противопоказаний с учетом соблюдения осторожности. Подчеркивается особая важность вакцинации при наличии:
- множественных сосудистых осложнений;
- коморбидной кардиоваскулярной патологии;
- хронической болезни почек, особенно в терминальной стадии, включая пациентов после трансплантации почки.
Наряду с общими противопоказаниями к вакцинации дополнительные противопоказания для пациентов с СД включают острые осложнения СД (диабетический кетоацидоз, гиперосмолярное состояние, лактацидоз и тяжелая гипогликемия).
Рекомендуется соблюдать осторожность при проведении вакцинации у пациентов с выраженной декомпенсацией (гипергликемия более 13 ммоль/л или HbAlc 8,5). Решение о проведении вакцинации должно быть принято врачом после общего осмотра пациента и анализа дневника самоконтроля.
После вакцинации рекомендовано проведение самоконтроля гликемии не менее 3-х раз в сутки, при необходимости, коррекция используемых доз инсулина. При СД 1 типа коррекция проводится за счет увеличения дозы инсулина короткого действия на 10% от исходной дозы (+1-2МЕ).
Оптимальные целевые показатели: глюкоза плазмы от 4 до 8 ммоль/л, HbAlc: менее 7%; для постоянного мониторинга: время в пределах глюкозы (3.9-10 ммоль/л): более 70% или для пожилых >50%. Пожилым пациентам рекомендуется деинтенсификация терапии во избежание гипогликемий (целевой уровень глюкозы крови натощак 5,010,0 ммоль/л и 6,1-11,1 ммоль/л перед сном). Аналогичные рекомендации распространяются на пациентов с ожирением.
Патология щитовидной железы - согласно мнениям экспертов вакцинация не противопоказана. Группу особого риска составляют пациенты с аутоиммунной офтальмопатией, получающие иммуносупрессивную терапию. Эта категория пациентов должна иметь приоритет в вакцинации.
Болезнь Грейвса, токсический многоузловой зоб, аутоиммунный тиреоидит, узловой зоб, простой нетоксический зоб не являются противопоказаниями для вакцинации.
Надпочечниковая недостаточность любой этиологии (первичная и вторичная) - патология, существенно ухудшающая прогноз при COVID-19, так как может привести к развитию адреналового криза. При надпочечниковой недостаточности пациенты должны иметь приоритет в вакцинации и знать о правилах «больничных дней», т.е. увеличить дозу используемых глюкокортикоидов в 2 раза на 2-3 дня для профилактики аддисонического криза.
Гипопаратиреоз и сопровождающая его потенциальная
гипокальциемия увеличивают риск негативных исходов COVID-19, поэтому пациенты с этой патологией также нуждаются в вакцинации в первую очередь.
Вертебральные переломы у пациентов с любым генезом остеопороза - доказанный фактор риска негативного прогноза при инфекции COVID-19, что определяет актуальность вакцинации лицам с вертебральными переломами.
Заболевания гипофиза, гиперпаратиреоз, все формы гипогонадизма не являются противопоказаниями для вакцинации против COVID-19. В случаях, когда при заболеваниях гипофиза имеется вторичная надпочечниковая недостаточность, вакцинация становится приоритетной.
Раздел 5. Вакцинация против COVID-19 лиц с заболеваниями сердечно-сосудистой системы
На состоявшемся в мае 2021 года совещании Евразийских экспертов по поводу постковидного синдрома у кардиологических пациентов показано, что имеет место резкое увеличение сердечно-сосудистой заболеваемости и смертности после перенесенного COVID-19. Представлены данные свидетельствующие о том, что после перенесенного COVID-19 у лиц, ранее не имевших патологию со стороны сердца зарегистрировано увеличение впервые зарегистрированных заболеваний сердечно-сосудистой системы.
Справочно: По данным наблюдения ГУ «РНПЦ Кардиологии» за 196 пациентами, не имевшими ранее диагностированных сердечнососудистых заболеваний, свидетельствуют о том, что через 6 месяцев после перенесенной инфекции COVID-19 у них сохраняется клиническая симптоматика со стороны сердечно-сосудистой системы, значимо влияющая на качество их жизни.
Это касается в том числе и пациентов, которые перенесли инфекцию в легкой или бессимптомной форме. Те реологические изменения, которые у них возникают, персистирование вируса в кардиомиоцитах и эндотелии приводят к аритмии, сердечно-сосудистой недостаточности и другим проблемам (https://doi.org/l0.W38/e4l37l-020-0387-4). Поэтому эта категория пациентов должна быть в поле зрения специалистов, и вопросы вакцинации этой категории пациентов особенно актуальны.
Пациенты с сердечно-сосудистой патологией приоритетно должны получить вакцинацию против COVID-19 по следующим причинам (Andrade Vartines et al. Vaccinating Patients with Heart Diseases Against COVID-19. The reasons for Priority. DO% https ://doi. or Cl 0.36660/abc/20210012):
инфекция сопровождается системным воспалением, что может обострить все проявления сердечно-сосудистой патологии, имеющиеся у пациента и спровоцировать новые состояния;
COVID-19 сопровождается дыхательной недостаточностью, что может спровоцировать у пациентов инфаркт миокарда 2 типа, церебральную патологию, которая по отдельным публикациям доминирует как причина смертности, почечную недостаточность; протромботический статус типичен для COVID-19, что создает множественные острые сердечно-сосудистые катастрофы и т.д.
Влияние COVID-19 на сердечно-сосудистую систему чрезвычайно многообразно. Это и острый коронарный синдром, и повреждение миокарда, и аритмии, и прогрессирование сердечной недостаточности, и выпот в полости перикарда, и тробоэмболические осложнения (в том числе, тромбоз стента). В основе большинства из них лежит такой фактор как COVID-19-ассоциированная коагулопатия. По данным ГУ «РНПЦ Кардиология» у 100% умерших пациентов этот феномен имел место. Наибольший удельный вес приходился на тромбоэмболию легочной артерии (45,5%). И если у такого пациента возникает повторное заболевание COVID-19, то шансы на благоприятный исход у него значительно ниже, чем у других пациентов (Митъковская Н.А., Плешко А.А. и др., 2021).
ПРЕДЛОЖЕНИЯ ПО ВЫДЕЛЕНИЮ УРОВНЕЙ ПРИОРИТЕТА ВАКЦИНАЦИИ ДЛЯ
ЛИЦ С СЕРДЕЧНО-СОСУДИСТЫМИ ЗАБОЛЕВАНИЯМИ

Вакцинацию каждому такому пациенту необходимо назначать индивидуально, учитывая тяжесть состояния на текущий момент. Носле проведенной вакцинации необходимо обеспечить контроль за их состоянием.
Пациентам, перенесшим острый инфаркт миокарда по истечении острого периода (на этапе подострого периода или постинфарктного кардиосклероза), пациентам с сердечной недостаточностью класса III-IV по NYHA, пациентам после трансплантации сердца, пациентам с патологией клапанов (в том числе, с критическим стенозом аортального клапана) целесообразно приоритетное назначение вакцинации. Но при этом необходимо сопоставлять риск возникновения тяжелой инфекции с риском возникновения поствакцинальных реакций и осложнений.
Раздел 6. Вакцинация против COVID-19 лиц с онкологическими заболеваниями
Несмотря на отсутствие ретроспективных сравнительных исследований онкологических и неонкологических пациентов,
многочисленные наблюдения свидетельствуют, что онкологические пациенты подвержены риску развития более тяжелого течения COVID-19. В частности, это относится к пациентам с онкогематологическими заболеваниями, злокачественными опухолями легких и диссеминированными злокачественными заболеваниями. Также повышен риск инфицирования у пациентов с солидными опухолями в первый год после постановки диагноза и снижается до общего популяционного уровня у пациентов, находящихся в ремиссии более 5 лет после установления онкологического диагноза.
По данным реестра COVID-19 и Cancer Consortium (ССС19) показатель летальности в этой группе пациентов колебался по данным мета-анализа до 26% и был выше по сравнению со всем населением (23%).
Имеющиеся данные о вакцинации против гриппа у онкологических пациентов позволяют предполагать развитие иммунного ответа на вакцины против COVID-19, а на его выраженность может влиять ряд факторов (морфология злокачественной опухоли, вид противоопухолевого лечения и его временные рамки, иммунологический статус и общее состояние пациента). Ретроспективные данные указывают на хорошую переносимость и безопасность вакцинации против гриппа у онкологических пациентов, получающих ингибиторы PD-1 или PD-L1, а также у пациентов, проходящих химиотерапию или таргетную терапию.
Как подчеркивает Европейское общество клинических онкологов, существует достаточно доказательств в поддержку вакцинации против COVID-19 онкологических пациентов, включая пациентов, проходящих иммуносупрессивную терапию (за исключением использования живых и векторных вакцин, способных к репликации).
Вакцины против вируса SARS-CoV-2 доказали свою безопасность и эффективны в общей популяции. Дополнительные поствакцинальные реакции у онкологических пациентов до сих пор не описаны. Как подчеркивает Европейское общество клинических онкологов, преимущества вакцинации превышают риски. Вакцинация этой группы пациентов должна быть приоритетной, независимо от других показаний, таких как, например, возраст.
Нет опубликованных данных об иммуногенности и взаимодействии мРНК-содержащих вирусных вакцин с противоопухолевой терапией у онкологических пациентов. Вакцины на основе мРНК против неинфекционных заболеваний (например, меланомы) тестировались на онкологических пациентах в течение последних 10 лет и не вызывали особых опасений по поводу безопасности. У пациентов, получавших в течение последних 6 месяцев противоопухолевое лечение, влияющее на
Целесообразно организовать рассмотрение вопроса о вакцинации контактов онкологических пациентов (это члены семьи, опекуны или близкие родственники) - так называемый эффект «кокона». Тем самым, В-лимфоциты (анти CD20-, анти CD19-, анти CDlO-моноклональные антитела, терапия CAR-T CD 19), может наблюдаться снижение защитного эффекта вакцины из-за субоптимального иммунного ответа.
Уровень эффективности может быть снижен в некоторых популяциях онкологических пациентов с интенсивной иммуносупрессией, например, у пациентов после трансплантации гемопоэтических клеток. При отсутствии признаков болезни вакцину можно использовать через 3-6 месяцев после трансплантации.
Эффективность вакцин против COVID-19 может варьировать у пациентов в зависимости от типа и течения злокачественного процесса (вида и распространенности опухолевого заболевания, вторичной иммуносупрессии, вызванной опухолью или лечением). Следуя Инструкции к лекарственному средству Гам-КОВИД-Вак, комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 у пациентов, получающих иммуносупрессивную терапию и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан 14-30 дней до и после вакцинации из-за риска снижения иммуногенности.
Существует три категории онкологических пациентов, у которых следует рассматривать вопросы вакцинации:
пациенты с активным опухолевым заболеванием и получающие противоопухолевое лечение;
пациенты с хроническим течением опухолевого заболевания после активного противоопухолевого лечения в стадии стабилизации/ремиссии;
пациенты, получившие радикальное лечение и не имеющие признаков возврата болезни.
Хотя потребность в вакцинации очевидна для первых двух категорий, рекомендуется также вакцинировать пациентов, получивших радикальное лечение и не имеющих признаков возврата болезни (особенно онкогематологических пациентов).
Сроки вакцинации зависят от индивидуального плана лечения. В идеале вакцинацию следует проводить до начала системного противоопухолевого лечения. Однако, если пациент уже начал системное лечение, вакцинация при ее доступности во время терапии может быть оправдана, взвесив все риски и пользу. Оптимальное время вакцинации по отношению к циклам химиотерапии не определено.
мы минимизируем риск заражения SARS-CoV-2 в семье (месте проживания), где имеется наибольший риск заражения.
Согласно рекомендациям Комитета по вакцинации NCCN должен быть приоритет вакцинации против COVID-19 перед другими вакцинами, между вакцинацией COVID-19 и другими одобренными вакцинами рекомендуется 14 дней.
Рекомендации CDC по срокам вакцинации после заражения COVID- 19: после прекращения изоляции (>20 дней для онкологических пациентов) и/или наличие nocT-SARS-CoV-2 специфичных моноклональных антител или использования плазмы выздоравливающих COVID-19 (через 90 дней).
Комитет по вакцинации NCCN признает, что гранулоцитопения сама по себе существенно не влияет на иммунологический ответ после вакцинации. Он используется в условиях глубокой иммуносупрессии у пациентов с онкогематологическими злокачественными новообразованиями в качестве суррогатного маркера восстановления адекватной иммунокомпетентности для ответа на вакцины и достаточного восстановления тромбоцитов, чтобы избежать кровотечения при внутримышечном введении вакцины. Это не используется для определения сроков вакцинации при лечении солидных злокачественных опухолей из-за коротких периодов нейтропении.
У пациентов, получающих химиотерапию, оптимальное время вакцинации по отношению к циклам химиотерапии неизвестно. Вариабельность конкретных схем и интервалов между циклами не позволяет утверждать, будет ли вакцинация более эффективна при введении во время химиотерапии по сравнению с серединой цикла, когда количество лейкоцитов может оказаться наименьшим. При отсутствии данных Комитет рекомендует вакцинацию, если таковая возможна. Существует теоретический риск обострения иммуноопосредованных побочных эффектов у пациентов, получающих ингибиторы иммунных контрольных точек. Данных о сроках введения вакцины при
иммунотерапии нет, поэтому для удобства это можно рассматривать в тот же день, что и иммунотерапия, при этом по возможности сократить количество дополнительных посещений.
Основная причина отказа от вакцинации в периоперационный период связана с тем, что симптомы (например, лихорадка) могут маскировать как послеоперационные осложнения, так и поствакцинальные. При более сложных операциях (например, спленэктомия или операции, которые могут привести к иммуносупрессивному состоянию) хирурги могут рекомендовать более длительный период (+/- 2 недели) с момента операции.
После вакцинации необходимо тщательное наблюдение за онкологическими пациентами для оценки потенциальных побочных эффектов и клинических исходов, например, инфекции, тяжести и смертности от COVID-19, онкологических осложнений и т.д.
Раздел 7. Вакцинация против COVID-19 лиц с различными заболеваниями
7.1. Можно проводить вакцинацию лицам с рассеянным склерозом?
Можно и нужно. Риск повышения активности процесса после вакцинации против COVID-19 не выявлен (выборка 435 пациентов). Безопасность аналогична общей популяции. Эффективность зависит от схемы лечения (АсШгоп, A etal. Mult Scler. 2021 May;27(6):864-870).
7.2. Можно ли вакцинировать лиц с хронической почечной недостаточностью?
У лиц с хронической почечной недостаточностью, в том числе находящихся на гемодиализе, а также у лиц после трансплантации почки после вакцинации против COVID-19 безопасность по профилю общей популяции. Эффективность обратно коррелирует с иммуносупрессией
7.3. Насколько целесообразно назначать вакцинацию лицам с хроническими вирусными гепатитами В или С, ВИЧ-инфекцией и туберкулезом?
Имеется достаточно данных, которые доказывают, что обострение хронического вирусного гепатита, ВИЧ-инфекция, туберкулез, а особенно коинфекция ВИЧ-инфекция+туберкулез (ТВ/ВИЧ) являются значительным риском утяжеления течения COVID-19 и риском летального исхода.
Время выздоровления от COVID-19 в случаях коинфекции COVID-19/TB может быть дольше, а тяжелые/критические симптомы COVID-19 могут быть преждевременными. SARS-CoV-2 может вызывать временное подавление клеточного иммунитета, что еще больше предрасполагает пациентов к реактивации или новой инфекции ТБ/ВИЧ (Jacques L. Tamizu et al. Implications of COVID-19 in high burden countries for HIV/ТВ: A sistimatic review of evidence, BMC INFECT DIS, 2020, 20:744).
Коинфицирование (COVID-19+ТБ) приводит к более быстрому развитию болезни в сравнении с пациентами без ТБ. Установлена возможность лекарственных взаимодействий, а также аддитивной гепатотоксичности (ремдисивир) из-за одновременного применения лекарственных средств для лечения туберкулеза и противовирусных лекарственных средств (Dr. Rohit Kumar el al. COVID-19 and ТВ co-infection - «Finishinh touch» in perfect recipe to «severity» or «death»: J.Infect 2020, sep.81 (3): e39-e40).
Вакцинация против COVID-19 таких пациентов целесообразна и безопасна. Эффективность коррелирует с иммуносупрессией
7.4. Можно вакцинировать лиц с аспириновой астмой?
Да, вакцинация таких пациентов может быть проведена при условии четкого контроля в течение 1 часа после введения вакцины.
Раздел 8. Техника введения и использования вакцины
8.1.Каково время разморозки компонентов вакцины Гам- КОВИД-Вак перед введением?
Опыт работы показал, что это время ориентировочно не превышает 30 минут при комнатной температуре.
8.2. Каков порядок использования в холодильном оборудовании (морозильной камере) термоиндикаторов?
Для регистрации температуры хранения вакцин могут использоваться прошедшие государственную поверку логгеры, терморегистраторы и другие электронные устройства. В соответствии с
требованиями части второй пункта 23 Надлежащей практики хранения лекарственных средств, утвержденной постановлением Министерства здравоохранения Республики Беларусь от 23 октября 2020 № 88 (далее - ННХ), при хранении термолабильных лекарственных средств необходимо обеспечить температурный режим, указанный на упаковке лекарственного средства, и его постоянный контроль в соответствии с пунктом 15 НПХ. Частью пятой пункта 15 ННХ предусмотрено, что оборудование (средства измерения) для контроля температуры должно быть размещено, по результатам анализа температурного картирования в точках наиболее значительного колебания температуры.
8.3. Какая максимальная температура хранения вакцины Г ам-КОВИД-Вак?
Оборудование, предназначенное для хранения и транспортировки вакцины Гам-КОВИД-Вак, должно обеспечивать температурный режим минус 18°С и ниже в течение всего времени транспортирования и хранения при любой допустимой степени загрузки.
8.4. Допустимо ли совместное хранение в одном морозильнике (ларе) вакцины и хладоэлементов?
Согласно части седьмой пункта 23 ННХ хладоэлементы могут размещаться с лекарственными средствами таким образом, чтобы отсутствовал прямой контакт с ними.














.jpg)










